 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知298K时,将反应Fe+2Fe3+=3Fe2+组成原电池,已知标准电极电势(Fe3+/Fe2+)=0.771V和(Fe2+/Fe)=-0.440V,则下列说法错误的是()。
A.电对Fe3+/Fe2+做正极
B.反应Fe+2Fe3+=3Fe2+的平衡常数大约为8×1040
C.电池组成式为(-)Fe|Fe2+(c1)||Fe2+(c2),Fe3+(c3)|Pt()
D.电池的标准电动势为0.331V
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.电对Fe3+/Fe2+做正极
B.反应Fe+2Fe3+=3Fe2+的平衡常数大约为8×1040
C.电池组成式为(-)Fe|Fe2+(c1)||Fe2+(c2),Fe3+(c3)|Pt()
D.电池的标准电动势为0.331V
 答案
答案
 更多“已知298K时,将反应Fe+2Fe3+=3Fe2+组成原电池,已知标准电极电势(Fe3+/Fe2+)=0.771V和(Fe2+/Fe)=-0.440V,则下列说法错误的是()。”相关的问题
更多“已知298K时,将反应Fe+2Fe3+=3Fe2+组成原电池,已知标准电极电势(Fe3+/Fe2+)=0.771V和(Fe2+/Fe)=-0.440V,则下列说法错误的是()。”相关的问题
第1题
根据下列反应组成电池
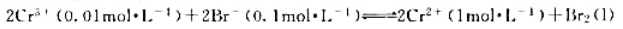
(1)写出电池符号;
(2)计算298K时的电动势,并判断反应自发进行的方向;
已知
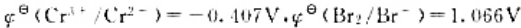
第3题
植物在光合作用中合成葡萄糖的反应可以近似表示为:
6CO2(g)+6H2O(1)=C6H12O6(s)+6O2(g)
计算反应的标准摩尔吉布斯自由能,判断反应在298K及标准状态下能否自发进行,已知葡萄糖的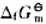 (C6H12O6·s) =-910.5kJ·mol-1。
(C6H12O6·s) =-910.5kJ·mol-1。
第4题
下列化学反应:NO2(g)+O3(g)=NO3(g)+O2(g)
在298K时,测得的数据如下表:

(1)求反应速率方程的表达式.
(2)求总反应的级数.
(3)求该反应的反应速率常数
第7题
已知某反应的活化能为70kJ·mol-1,300K时的速率常数为0.1s-1,试计算
(1)400K时,反应的速率为原来的多少倍?
(2)温度由1000K升高到1100K时,反应速率为1000K时的多少倍?
第11题
A.反应是可逆反应或可逆过程
B.正反应和逆反应速率相等
C.平衡时体系中反应物和生成物的浓度将不再改变
D.到达平衡状态,反应速度即为零,反应立即结束