 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
用简单的化学方法区分下列各组化合物。(1)戊醛,二乙酮,2-戊酮(2)二乙基缩乙醛,正丙醚,2-己醇(3)1,4-二氧六环和1,3,5-三氧六环(4)2-戊酮,乙酰丙酮,4-氧代戊醛
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 答案
答案
 更多“用简单的化学方法区分下列各组化合物。(1)戊醛,二乙酮,2-戊酮(2)二乙基缩乙醛,正丙醚,2-己醇(3)1,4-二氧六环和1,3,5-三氧六环(4)2-戊酮,乙酰丙酮,4-氧代戊醛”相关的问题
更多“用简单的化学方法区分下列各组化合物。(1)戊醛,二乙酮,2-戊酮(2)二乙基缩乙醛,正丙醚,2-己醇(3)1,4-二氧六环和1,3,5-三氧六环(4)2-戊酮,乙酰丙酮,4-氧代戊醛”相关的问题
第2题
【题目描述】
18.(10分)二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂。与Cl2相比ClO2不但具有更显著的杀菌能力,而且不会产生对人体有潜在危害的有机氯代物。
(1)在ClO2的制备方法中,有下列两种制备方法:
方法一:2NaClO3+4HCl===2ClO2↑+Cl2↑+2NaCl+2H2O
方法二:2NaClO3+H2O2+H2SO4===2ClO2↑+Na2SO4+O2↑+2H2O

用方法二制备的ClO2更适合用于饮用水的消毒,其主要原因是▲。
(2)用ClO2处理过的饮用水(pH为5.5~6.5)常含有一定量对人体不利的亚氯酸根离子的含量应不超过0.2mg·L-1。
饮用水中CIO2、CIO2的含量可用连续碘量法进行测定。CIO2被I-还原为CIO-2、Cl-的转化率与溶液pH的关系如右图所示。当pH≤2.0时,CIO-2也能被I-完全还原成Cl-。反应生成的I2用标准Na2S2O3溶液滴定: ①请写出pH≤2.0时,CIO-2与I-反应的离子议程式▲。 ②请完成相应的实验步骤: 步骤1:准确量取V mL水样加入到锥形瓶中。 步骤2:调节水样的pH为7.0~8.0。 步骤3:加入足量的KI晶体。 步骤4:加少量淀粉溶液,用c mol·L-1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V1mL。 步骤5:▲。 ③根据上述分析数据,测得该饮用水样中CIO-2的浓度为▲mol·L-1(用含字母的代数式表示。) ④若饮用水中ClO-2的含量超标,可向其中加入适量的Fe2+将ClO-2还原成Cl-, 该反应的氧化产物是▲(填化学式)。
(1)方法二制备的ClO2中不含Cl2

第3题
【题目描述】
5、今年,甲型H1N1流感病毒在许多国家发生,治疗该病毒的有效药物达菲是从八角茴香中经过多道复杂工艺提炼出来的,它的有效成分是莽草酸,化学式为C7H10O5.对莽草酸的下列说法错误的是()
A.莽草酸是有机化合物
B.莽草酸由碳、氢氧三种元素组成
C.莽草酸的相对分子质量为174
D莽草酸中含有7个碳原子、10个氢原子和5个氧原子
| 【我提交的答案】:C |
| 【参考答案与解析】: 正确答案:D |
答案分析:
【我的疑问】(如下,请求专家帮助解答)
分析一下D的选项
第4题
用柱面坐标或球面坐标把三重积分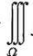 f(x,y,z)dV化为三次积分,其中Ω分别是由如下各组不等式所确定的区域:
f(x,y,z)dV化为三次积分,其中Ω分别是由如下各组不等式所确定的区域:
(1)z≥x2+y2,z≤2-√(x2+y2);
(2)x2+y2+z2≤a2,x2+y2+z2≤2az;
(3)x2+y2+z2≤a2,z2≤3(x2+y2);
(4)x2+y2+z2≤a2,x≥0,y≥0,z≤0。
第6题
A.采用有颜色的区域线及标识加以区分
B.分类标识及用颜色区分
C.标识出最大库存线、安全库存线
D.轨道方式(一头入,另一头出),斜坡方式(上入下出)
第9题
A.用物理方法和化学方法加速进行试验的方法
B.暴露自然条件下试验的方法
C.放置于使用现场进行试验的方法
D.放置人工模拟环境试验的方法